Antikörper-Engineering
Antikörperentwicklung durch Elektrochemie
- Elektrochemische Reduktion, Konjugation und Reoxidation von Antikörpern
- Grüne Technologie – Elektronen statt giftiger Chemikalien
- Selektiv – erzeugt leichte und schwere Ketten
- Schnell – Sekunden im Vergleich zu Stunden bei chemischen Verfahren (z. B. TCEP, DTT)
Dieser neuartige elektrochemische Ansatz bietet eine schnelle und effiziente Methode für die selektive Reduktion, Konjugation und Reoxidation von Antikörpern, ohne dass reduzierende Chemikalien benötigt werden. Die Reduktion von Antikörpern in ihre leichten Ketten (Lc) und schweren Ketten (Hc) wird mit der bereits veröffentlichten elektrochemischen Methode durchgeführt, die auf Rechteckpotentialimpulsen basiert, die an die von Antec entwickelte Ti-Elektrode angelegt werden. Anschließend kann das freie Cystein, das bei der elektrochemischen Reduktion des Antikörpers entsteht, konjugiert werden. Schließlich kann das freie Cystein sowohl auf Lc als auch auf Hc sehr schnell und selektiv reoxidiert werden, um den Antikörper in hoher Ausbeute neu zu bilden. Die elektrochemische Behandlung beeinträchtigte die Bindungsaffinität der Antikörper nicht und machte den Einsatz aggressiver Chemikalien und zusätzlicher mühsamer Reinigungsschritte überflüssig.
Für weitere Details: siehe auch unsere Technologie-Seite.
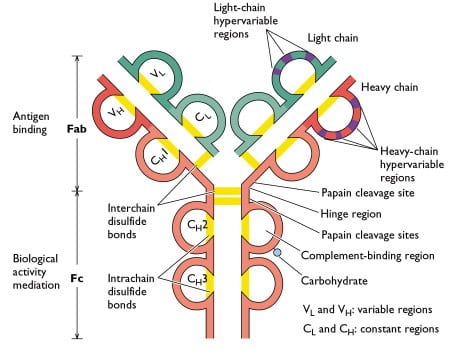
Grafische Darstellung eines Antikörpers mit Disulfidbindungen, die die schwere und die leichte Kette zusammenhalten. Das Aufbrechen einer Disulfidbindung in einem elektrochemischen Durchflussreaktor erfordert ein Potenzial von etwa -1 V.
Massenspektren
Die elektrochemische Reduktion von Disulfidbindungen dürfte sich als wichtiger technologischer Fortschritt erweisen, nicht nur bei der Analyse von Antikörpern, sondern auch bei der Entwicklung neuartiger Therapeutika auf Antikörperbasis, wie z. B. bi-spezifische Antikörper oder Antikörper-Wirkstoff-Konjugate. Die MS-Spektren unten zeigen die Reaktionsprodukte (Lc und Hc) nach dem Einschalten der Reaktorzelle (B und D).
Infusion einer angesäuerten Antikörperlösung in das Massenspektrometer bei ausgeschalteter μ-PrepCell (A) führte zu einer Ladungshüllkurve, die sich zwischen m/z 2200 und 4000 ausbreitet, wobei der intakte Antikörper etwa 40 bis 60 Ladungen trägt. Wenn die Zelle eingeschaltet wurde (B) wurde eine Verschiebung der Ladungshülle des Antikörpers zu niedrigeren m/z-Werten (~1000-2500) beobachtet.
Das Spektrum (C) ergibt sich aus der Entfaltung des MS-Signals (A), das mit der ausgeschalteten Zelle erhalten wurde, und bestätigt, dass der Antikörper intakt ist. D wurde bei eingeschalteter Zelle erhalten und zeigt hauptsächlich Spezies mit Molekulargewichten von etwa 25 und 50 kDa, die den Massen von Lc und Hc entsprechen. Die sehr geringe Intensität des MS-Signals für Spezies mit einem Molekulargewicht von mehr als 50 kDa bestätigt die selektive Reduktion der Antikörper-Zwischenkettendisulfidbindungen in hohen Ausbeuten.
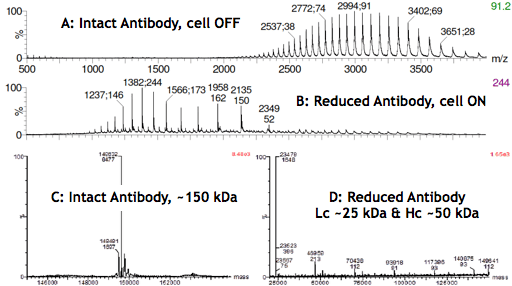
Hochauflösende Massenspektren eines monoklonalen Antikörpers vor/nach elektrochemischer Reduktion der Disulfidbindungen.
ELISA-Bindungstest
Die im ELISA für drei verschiedene Antikörper – in nativer Form (grün), elektrochemisch reduziert und reoxidiert (rot und blau) – erhaltenen Kurven zeigen eine hervorragende Übereinstimmung, die veranschaulicht, dass die elektrochemische Behandlung von Antikörpern weder ihre Bindungsaktivität noch ihre biologische Aktivität beeinträchtigt, selbst wenn der reduzierte Antikörper mehrere Stunden in saurem Medium gehalten wird.
Mit freundlicher Genehmigung: Daten zur Verfügung gestellt von Dr. Xin Cheng & Arielle Verdi (Morphotek Inc., Exton, PA).

Bewertung der Ligandenbindungsaffinität durch ELISA.
Elektrochemische Reaktoren für MS und Synthese
Stoffwechsel von Arzneimitteln
Abbaustudien
Lipidomik, Lipid-Oxidation
Applikationen
Poster