Ingeniería de anticuerpos
Ingeniería de anticuerpos por electroquímica
- Reducción electroquímica, conjugación y reoxidación de anticuerpos
- Tecnología verde: electrones en lugar de productos químicos tóxicos
- Selectiva – genera cadenas ligeras y pesadas
- Rápido – segundos frente a horas con enfoques químicos (por ejemplo, TCEP, DTT)
Este novedoso enfoque electroquímico proporciona un método rápido y eficaz para la reducción selectiva, conjugación y reoxidación de anticuerpos sin necesidad de productos químicos reductores. La reducción de los anticuerpos en sus cadenas ligeras (Lc) y pesadas (Hc) se realiza por el método electroquímico publicado anteriormente, basado en pulsos de potencial de onda cuadrada aplicados al electrodo de Ti patentado por Antec. Posteriormente, se puede conjugar la cisteína libre generada por la reducción electroquímica del anticuerpo. Por último, la cisteína libre tanto en Lc como en Hc puede reoxidarse muy rápida y selectivamente para reformar el anticuerpo en altos rendimientos. El tratamiento electroquímico no afectó a la afinidad de unión de los anticuerpos, al tiempo que eliminó la necesidad de utilizar productos químicos agresivos y los tediosos pasos de limpieza adicionales.
Para más detalles: consulte también nuestra página sobre tecnología.
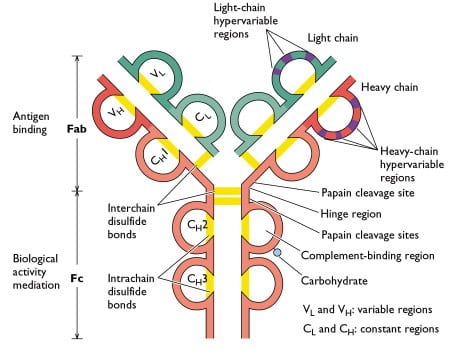
Representación gráfica de un anticuerpo con enlaces disulfuro que mantienen unidas las cadenas pesada y ligera. La ruptura de un enlace disulfuro en un reactor electroquímico de flujo continuo requiere un potencial de aproximadamente -1 V.
Espectro de masas
Es probable que la reducción electroquímica de los enlaces disulfuro se revele como un importante avance tecnológico no sólo en el análisis de anticuerpos, sino también en el diseño de nuevas terapias basadas en anticuerpos, como los anticuerpos biespecíficos o los conjugados anticuerpo-fármaco. Los siguientes espectros MS muestran los productos de reacción (Lc y Hc) tras encender la célula del reactor (B y D).
Infusión de una solución acidificada de anticuerpos en el espectrómetro de masas con el μ-PrepCell apagado. (A) dio lugar a una envoltura de carga que se extendía entre m/z 2200 y 4000, con el anticuerpo intacto portando aproximadamente de 40 a 60 cargas. Cuando la célula estaba encendida (B), se observó un desplazamiento de la envoltura de carga del anticuerpo hacia m/z inferiores (~1000-2500).
El espectro (C) resulta de la deconvolución de la señal MS (A) obtenida con la célula OFF y confirma que el anticuerpo está intacto. D se obtuvo con la célula encendida, y muestra principalmente especies con pesos moleculares de aproximadamente 25 y 50 kDa correspondientes a las masas de Lc y Hc. La muy baja intensidad de la señal de EM para especies con pesos moleculares superiores a 50 kDa confirma además la reducción selectiva de los enlaces disulfuro intercadena del anticuerpo en altos rendimientos.
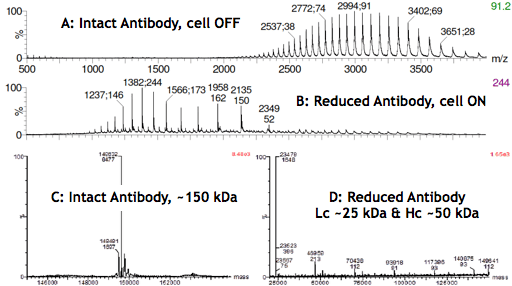
Espectros de masas de alta resolución de un anticuerpo monoclonal antes/después de la reducción electroquímica de los enlaces disulfuro.
Ensayo de unión ELISA
Las curvas obtenidas en ELISA para tres anticuerpos diferentes -en forma nativa (verde), electroquímicamente reducidos y reoxidados (rojo y azul)- muestran una excelente concordancia, lo que ilustra que el tratamiento electroquímico de los anticuerpos no afecta a su actividad de unión ni a su actividad biológica, incluso cuando se mantiene el anticuerpo reducido durante varias horas en medio ácido.
Cortesía: datos proporcionados amablemente por el Dr. Xin Cheng y Arielle Verdi (Morphotek Inc., Exton, PA).

Evaluación de la afinidad de unión del ligando mediante ELISA.